
Back Insulien Afrikaans إنسولين Arabic ইনছুলিন Assamese Insulina AST İnsulin Azerbaijani Insulin BAR Інсулін Byelorussian Інсулін BE-X-OLD Инсулин Bulgarian ইনসুলিন Bengali/Bangla
| Insulin | ||
|---|---|---|
| ||
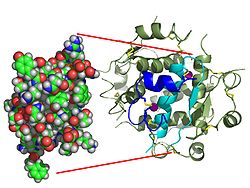
| Zwei Modelldarstellungen des Insulinmoleküls. Links das einfache Molekül (Monomer) als ein Kalottenmodell, aus dem die Oberflächenform hervorgeht. Rechts das sechsfache Molekül (Hexamer) als so genanntes Bändermodell, bei dem die innere Struktur deutlich wird. Bei letzterem sind α-Helices durch Schrauben und β-Faltblätter durch Pfeile dargestellt. | ||
|
Vorhandene Strukturdaten: 1ai0, 3ins, 4ins, 6ins, 7ins, 9ins | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 5,8 kDa[1] / 51 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Heterodimer (21 + 30 aa) | |
| Präkursor | Proinsulin | |
| Bezeichner | ||
| Gen-Name | INS | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | A10AB01 | |
| DrugBank | DB00030 | |
| Vorkommen | ||
| Homologie-Familie | CLU_140421_1_0 | |
| Übergeordnetes Taxon | Wirbeltiere | |
| Orthologe | ||
| Mensch | Maus | |
| Entrez | 3630 | 16334 |
| Ensembl | ENSG00000129965 | ENSMUSG00000000215 |
| UniProt | P01308 | Q5EEX1 |
| Refseq (mRNA) | NM_000207 | NM_008387 |
| Refseq (Protein) | NP_000198 | NP_032413 |
| Genlocus | Chr 11: 2.14 – 2.14 Mb | Chr 7: 142.49 – 142.49 Mb |
| PubMed-Suche | 3630 | 16334
|
Insulin (andere Namen: Insulinum, Insulinhormon, Inselhormon) ist ein für alle Wirbeltiere lebenswichtiges Proteohormon (Polypeptidhormon), das in den β-Zellen der Bauchspeicheldrüse gebildet wird. Diese spezialisierten Zellen befinden sich in den Langerhans-Inseln. Von diesen „Inseln“ leitet sich auch der Name „Insulin“ ab (von lateinisch insula „Insel“). Das seit 1921 bekannte Insulin ist an der Regulation des Stoffwechsels, insbesondere dem der Kohlenhydrate, beteiligt. Insulin senkt den Blutzuckerspiegel, indem es Körperzellen dazu anregt, Glucose aus dem Blut aufzunehmen.
- ↑ Matthias Otto: Analytische Chemie. John Wiley & Sons, 2011, ISBN 978-3-527-32881-9, S. 557.