Back Kalium Afrikaans ፖታሺየም Amharic Potasio AN पोटैशियम ANP بوتاسيوم Arabic پوطاسيوم ARY بوتاسيوم ARZ Potasiu AST पोटासियम AWA Kalium Azerbaijani
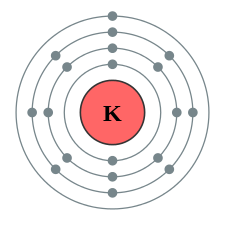
Kalium är ett grundämne och spårämne. Kalium tillhör gruppen alkalimetaller och är vanligt förekommande i naturen.
Kalium oxideras hastigt i luften, och är mycket reaktivt med vatten. Därför förvaras ren kaliummetall i någon typ av olja, såsom fotogen, för att förebygga oxidation. I naturen förekommer ofta kalium bundet till salt i till exempel havet, men det förekommer också i olika mineralföreningar. Ett flertal kaliumföreningar är vattenlösliga men kristalliserar sällan med hydratiseringsvatten[8] och används ofta i industrin.
Det är ett viktigt spårämne för djur och växter, där det verkar på cellnivå och vid överföring av nervsignaler. I människor reglerar kalium vatten-syrabalansen och vätskebalans. I muskelvävnadernas cellvätska är kalium den viktigaste katjonen.[9] Brist på kalium kallas hypokalemi och patologiskt höga värden kallas hyperkalemi.
- ^ CIAAW, Standard Atomic Weights Revised 2013.
- ^ Haynes, William M., red (2011). CRC Handbook of Chemistry and Physics (92nd ed.). Boca Raton (FL): CRC Press. ISBN 1439855110.
- ^ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Festkörper. 2:a uppl. De Gruyter, Berlin 2005, ISBN 978-3-11-017485-4 Lehrbuch der Experimentalphysik, volym 6, S. 361.
- ^ David R. Lide (red.): Electrochemical Series, sid. 8:22, i: CRC Handbook of Chemistry and Physics, uppl. 90 (internetversion: 2010), CRC Press / Taylor and Francis.
- ^ Magnetic susceptibility of the elements and inorganic compounds Arkiverad 12 januari 2012 hämtat från the Wayback Machine., in Lide, David R., red (2005). CRC Handbook of Chemistry and Physics (86th ed.). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5
- ^ Weast, Robert C. (ed. in chief): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990. Sidorna E-129 till E-145. ISBN 0-8493-0470-9. De angivna värdena har här räknats om enligt SI.
- ^ [a b] Referensfel: Ogiltig
<ref>-tagg; ingen text har angivits för referensen med namnetCLP_8150 - ^ Gunnar Hägg 1963, Allmän och oorganisk kemi, kapitel 25-1 sid 607
- ^ ”Arkiverade kopian”. Arkiverad från originalet den 4 mars 2016. https://web.archive.org/web/20160304113609/http://mesh.kib.ki.se/swemesh/show.swemeshtree.cfm?Mesh_No=D01.268.549.550&tool=karolinska. Läst 20 september 2011.