
Back Kalium Afrikaans ፖታሺየም Amharic Potasio AN पोटैशियम ANP بوتاسيوم Arabic پوطاسيوم ARY بوتاسيوم ARZ Potasiu AST पोटासियम AWA Kalium Azerbaijani
| Potassi | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
19K
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| Aspecte | |||||||||||||||||||||||||||||||
Gris argentat Perles de potassi en oli de parafina (la grossa fa 0,5 cm)  Línies espectrals del potassi | |||||||||||||||||||||||||||||||
| Propietats generals | |||||||||||||||||||||||||||||||
| Nom, símbol, nombre | Potassi, K, 19 | ||||||||||||||||||||||||||||||
| Categoria d'elements | Metalls alcalins | ||||||||||||||||||||||||||||||
| Grup, període, bloc | 1, 4, s | ||||||||||||||||||||||||||||||
| Pes atòmic estàndard | 39,0983(1) | ||||||||||||||||||||||||||||||
| Configuració electrònica | [Ar] 4s1 2, 8, 8, 1 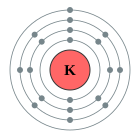
| ||||||||||||||||||||||||||||||
| Propietats físiques | |||||||||||||||||||||||||||||||
| Fase | Sòlid | ||||||||||||||||||||||||||||||
| Densitat (prop de la t. a.) |
0,862 g·cm−3 | ||||||||||||||||||||||||||||||
| Densitat del líquid en el p. f. |
0,828 g·cm−3 | ||||||||||||||||||||||||||||||
| Punt de fusió | 336,53 K, 63,38 °C | ||||||||||||||||||||||||||||||
| Punt d'ebullició | 1.032 K, 759 °C | ||||||||||||||||||||||||||||||
| Punt triple | 336,35 K (63 °C), kPa | ||||||||||||||||||||||||||||||
| Entalpia de fusió | 2,33 kJ·mol−1 | ||||||||||||||||||||||||||||||
| Entalpia de vaporització | 76,9 kJ·mol−1 | ||||||||||||||||||||||||||||||
| Capacitat calorífica molar | 29,6 J·mol−1·K−1 | ||||||||||||||||||||||||||||||
| Propietats atòmiques | |||||||||||||||||||||||||||||||
| Estats d'oxidació | 1 (òxid bàsic fort) | ||||||||||||||||||||||||||||||
| Electronegativitat | 0,82 (escala de Pauling) | ||||||||||||||||||||||||||||||
| Energies d'ionització (més) |
1a: 418,8 kJ·mol−1 | ||||||||||||||||||||||||||||||
| 2a: 3.052 kJ·mol−1 | |||||||||||||||||||||||||||||||
| 3a: 4.420 kJ·mol−1 | |||||||||||||||||||||||||||||||
| Radi atòmic | 227 pm | ||||||||||||||||||||||||||||||
| Radi covalent | 203±12 pm | ||||||||||||||||||||||||||||||
| Radi de Van der Waals | 275 pm | ||||||||||||||||||||||||||||||
| Miscel·lània | |||||||||||||||||||||||||||||||
| Estructura cristal·lina | Cúbica centrada en la cara 
| ||||||||||||||||||||||||||||||
| Ordenació magnètica | Paramagnetic | ||||||||||||||||||||||||||||||
| Resistivitat elèctrica | (20 °C) 72 nΩ·m | ||||||||||||||||||||||||||||||
| Conductivitat tèrmica | 102,5 W·m−1·K−1 | ||||||||||||||||||||||||||||||
| Dilatació tèrmica | (25 °C) 83,3 µm·m−1·K−1 | ||||||||||||||||||||||||||||||
| Velocitat del so (barra prima) | (20 °C) 2.000 m·s−1 | ||||||||||||||||||||||||||||||
| Mòdul d'elasticitat | 3,53 GPa | ||||||||||||||||||||||||||||||
| Mòdul de cisallament | 1,3 GPa | ||||||||||||||||||||||||||||||
| Mòdul de compressibilitat | 3,1 GPa | ||||||||||||||||||||||||||||||
| Duresa de Mohs | 0,4 | ||||||||||||||||||||||||||||||
| Duresa de Brinell | 0,363 MPa | ||||||||||||||||||||||||||||||
| Nombre CAS | 7440-09-7 | ||||||||||||||||||||||||||||||
| Isòtops més estables | |||||||||||||||||||||||||||||||
| Article principal: Isòtops del potassi | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
El potassi és l'element químic de símbol K i nombre atòmic 19. És un metall blanc argentat tan tou que es pot tallar amb un ganivet sense dificultat. Té un baix punt de fusió i és bon conductor tèrmic i de l'electricitat.[1]
És abundant en la natura, per exemple a l'aigua de mar (que conté un 0,04% de potassi en massa[2]) o en minerals diversos, com l'ortosa. S'oxida ràpidament en l'aire, és molt reactiu, especialment en aigua, i s'assembla químicament al sodi. És un element químic essencial per a la vida. Té un rol fonamental en la propagació dels impulsos nerviosos. La principal aplicació industrial del potassi és el seu ús en la fabricació d'adobs. Altres usos aprofiten l'elevada solubilitat aquosa dels compostos de potassi, per exemple, per a la fabricació de sabons.[3]
- ↑ Augustyn, Adam. «Potassium/ Chemical element». A: Encyclopedia Britannica [Consulta: 27 novembre 2019]. Arxivat 2019-07-09 a Wayback Machine.
- ↑ Webb, D. A. «The Sodium and Potassium Content of Sea Water». The Journal of Experimental Biology, 2, 4-1939, pàg. 183. Arxivat de l'original el 2019-09-24 [Consulta: 27 novembre 2019].
- ↑ Greenwood, p. 73